本博客由科研AI Agent实验室BenszResearch强力驱动!如何更快地访问本站?有需要可加电报群获得更多帮助。本博客用什么VPS?创作不易,请支持苯苯!推荐购买本博客的VIP喔,10元/年即可畅享所有VIP专属内容!
概览
- 本文围绕 前言 展开详细讨论
- 包含 30 个主要章节内容
- 文末提供总结与展望
前言
此文内容目前处于BETA版本
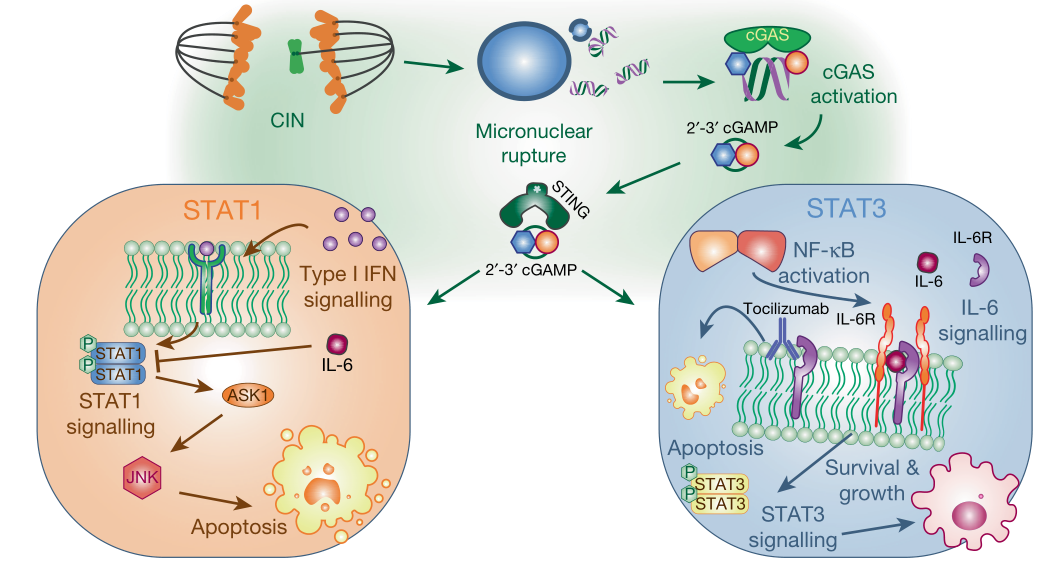
论文:cGAS–STING drives the IL-6-dependent survival of chromosomally instable cancers. Nature. 2022
From 荷兰-格罗宁根大学医学中心-欧洲老年生物学研究所的Floris Foijer团队.
全文资源:full.pdf.local; full.pdf.remote
此文还有Nature评论:Targeting cancers with chromosome instability. Nat Rev Drug Discov. 2022
Received: 1 September 2021;Accepted: 10 May 2022.
技术
Cell lines
- BT549:TNBC细胞株之一
- KIF2C (CIN low ) or dnMCAK (CIN high ) WT: 在本文中,KIF2C细胞一般指高表达MCAK(也称为KIF2C)的TNBC 4T1细胞,而dnMCAK细胞一般指高表达无功能MCAK突变型的TNBC 4T1细胞 。
inhibitors/drugs
- WEE1 inhibitor AZD1775 / MPS1 inhibitor reversine: 诱导微核形成并激活cGAS-STING通路。在本研究中,作者发现AZD1775治疗对BT549-WT也有一定的杀伤效应;但Reversine对BT549-WT则无明显杀伤效应,相对而言是比较接近临床的CIN诱导剂(毕竟临床观察到的CIN肿瘤肯定是正常生长状态)。
- Tocilizumab: 托珠单抗;interleukin-6 receptor (IL-6R)抑制剂
- RU.521: RU.521是cGAS(环状GMP-AMP合酶,cGAMP合酶)的小分子抑制剂。 cGAS 是胞质双链 DNA (dsDNA) 的主要传感器。cGAS通过STING和TBK1激活 I 型干扰素 (IFN)。
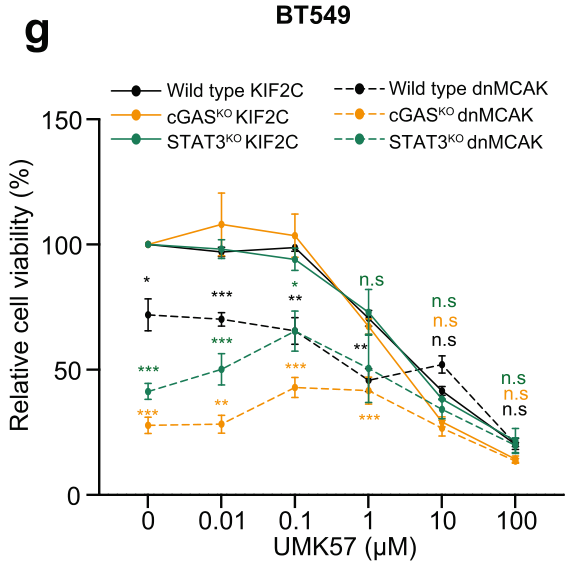
- UMK57 :详见ref。UMK57通过增强MCAK 的活性抑制CIN癌细胞中的染色体错误分离。亚致死剂量的UMK57 会在有丝分裂过程中破坏动粒-微管 (k-MT) 附件的稳定性,从而提高染色体分离保真度。令人惊讶的是,UMK57 处理的癌细胞中染色体错误分离会在几天内反弹。这种快速复发是由超稳定k-MT附件的Aurora B信号通路的改变驱动的,并且在 UMK57 去除后是可逆的。在本文中,UMK57主要用于在dnMCAK细胞中提高有丝分裂保真度(mitotic fidelity)。在较低剂量时(<0.1μM),UMK57可通过抑制CIN增强cGASKO/STAT3KOdnMCAK细胞的活力,这反证了CIN和cGAS信号抑制可产生合成致死性效应(这个说法可能不太严谨,但理是这个理, Extended Data Fig. 5g):
Animals
Lck-Cre品系可在胸腺细胞中特异性重组loxP侧翼等位基因
- Msh2 –/–(eT) mice: 产生非CIN型急性T细胞性白血病(T-ALL)
- Mad2 fl/fl ;Trp53 fl/fl ; Lck-cre mice用于构造CIN型急性T细胞性白血病
- Mps1 fl/fl ;Trp53 fl/fl ; Lck-cre mice用于构造CIN型急性T细胞性白血病
Experiments
- 有丝分裂异常定量:Quantification of mitotic abnormalities
- DNA纤维检测:DNA fibre assay;反映replication stress。可看这里了解详细。
- H2B–GFP–T2A–CENPB染色:For the quantification of kinetochores(动粒, 有丝分裂和减数分裂期间将染色体连接到微管聚合物上) in micronuclei, BT549 cells expressing histone H2B–GFP–T2A–CENPB (Centromere Protein B, 着丝粒蛋白B)–mCherry(着丝粒阳性微核) were seeded on a four-section imaging chamber and treated with 250 nM reversine or 500 nM AZD1775 24 h before imaging.
预备知识
cGAS-STING信号通路
Representative ref: DNA sensing by the cGAS–STING pathway in health and disease. Nat Rev Genet.2019. full.pdf.remote
Micronuclei 微核
Chromothripsis from DNA damage in micronuclei. Nature. 2015
NF-kappa-B信号通路
参考并引用自:https://www.cellsignal.cn/pathways/nfkb-signaling-pathway。本文的研究涉及到经典与非经典两种NF-kappa-B通路
NF-kappa-B 是由含有 Rel 样结构域的蛋白质 RELA/p65、RELB、NFKB1/p105、NFKB1/p50、REL 和 NFKB2/p52 形成的同源或异源二聚体复合物。异二聚体 RELA-NFKB1 复合物可能是最丰富的一种NF-kappa-B二聚体。二聚体在其靶基因的DNA 中的kappa-B位点结合,并且各个二聚体对不同的 kappa-B 位点具有不同的偏好,它们可以以可区分的亲和力和特异性结合这些位点。不同的二聚体组合分别充当转录激活剂或阻遏剂。
在经典信号通路中,NF-κB/Rel 蛋白与 IκB 蛋白结合并受到其抑制。促炎细胞因子、脂多糖 (LPS) 、生长因子以及抗原受体激活一个 IKK 复合体(IKKβ、IKKα 和 NEMO),后者将 IκB 蛋白磷酸化。IκB 磷酸化导致其自身泛素化以及蛋白酶体降解,释放 NF-κB/Rel 复合体。活性 NF-κB/Rel 复合体进一步由翻译后修饰(磷酸化、乙酰化、糖基化)作用激活,并转运入胞核,在核内单独或联合其他转录因子,包括 AP-1、Ets 和 Stat,并共同诱导靶标基因表达。
在非经典NF-κB 通路中,NF-κB2 p100/RelB 复合体在细胞浆中失活。信号转导通过受体的一个子集,包括 LTβR、CD40 和 BR3,激活激酶 NIK,而 NIK 反过来激活 IKKα 复合体,后者将 NF-κB2 p100 的 C 端残基磷酸化。NF-κB2 p100 的磷酸化导致其自身泛素化,并且蛋白酶体加工为 NF-κB2 p52。这样可产生具备转录能力的 NF-κB p52/RelB 复合体,并转运入胞核,再诱导目的基因表达。
结果
cGAS-STING信号缺失可抑制CIN型TNBC增殖
发现现象
MPS1/WEE1抑制诱导染色体不稳定性(CIN)的过程中,BT549细胞携带有丝分裂异常事件的比例会大大增加(a)。由于染色体不稳定性的增加,微核(micronuclei)的形成也很有可能大幅增加,相关的实验也证实了这一点(b-c)。与MPS1抑制(Reversine)不同,WEE1抑制(AZD1775)产生的微核着丝粒较少(d-e)并导致更大的复制压力(replication stress):
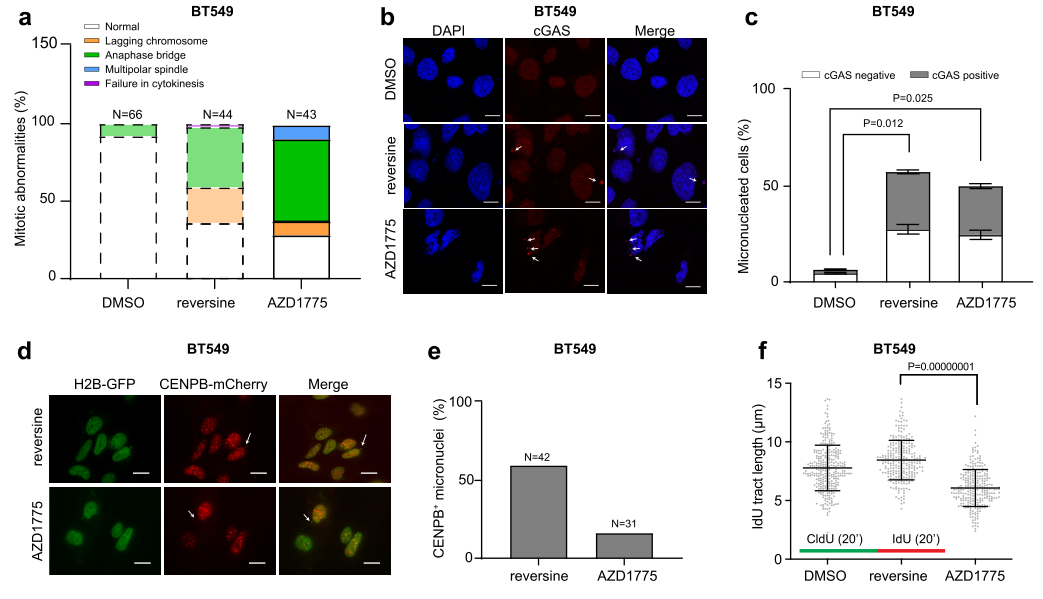
由于Reversine诱导BT549细胞CIN的过程可促进微核产生,因此研究者联想到胞浆DNA感受经典通路——cGAS-STING信号很可能也有所增强,这个猜测也得到了实验证实:

评估靶点
为了进一步评估cGAS-STING信号激活在CIN细胞中的重要性,研究者构建cGAS KO细胞株,并发现Reversine诱导CIN对cGAS KO BT549细胞的cGAS-STING信号强度无明显影响,其中包括胞内外cGAMP、:
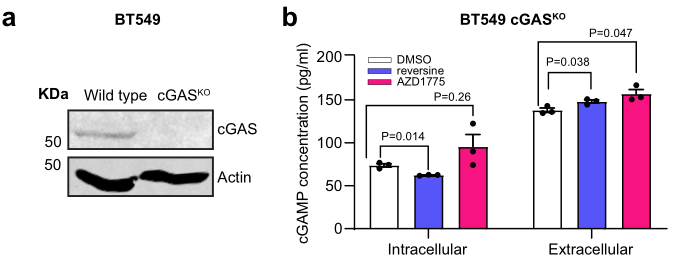
STING的表达水平:
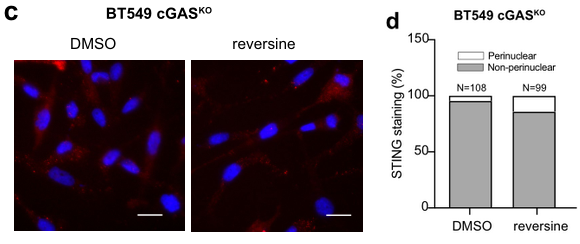
cGAS-STING下游——IRF3, STAT1 or STAT3的磷酸化:
这几个结果综合反映了cGAS KO株的cGAS-STING信号被成功阻断,并且CIN也无法激活。
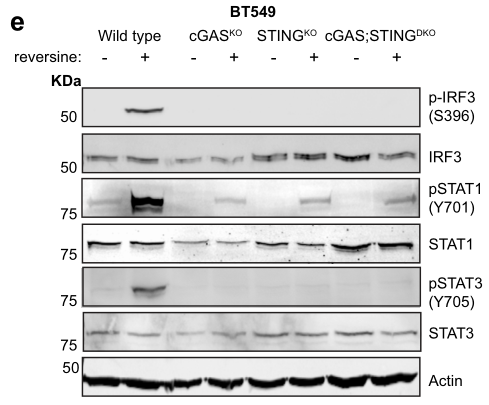
此外,Reversine诱导野生型BT549细胞CIN后,细胞生存能力不受明显影响;但是,此时如果敲除cGAS基因,CIN-BT549细胞的生存能力将显著减弱。这表明BT549细胞耐受CIN并生存的过程依赖cGAS信号:

研究者通过cGAS/STING-KO株、cGAS抑制剂(RU.521)等,结合体内外实验,证明Reversine/AZD1775诱导CIN过程中BT549细胞的生存是依赖cGAS/STING信号的:
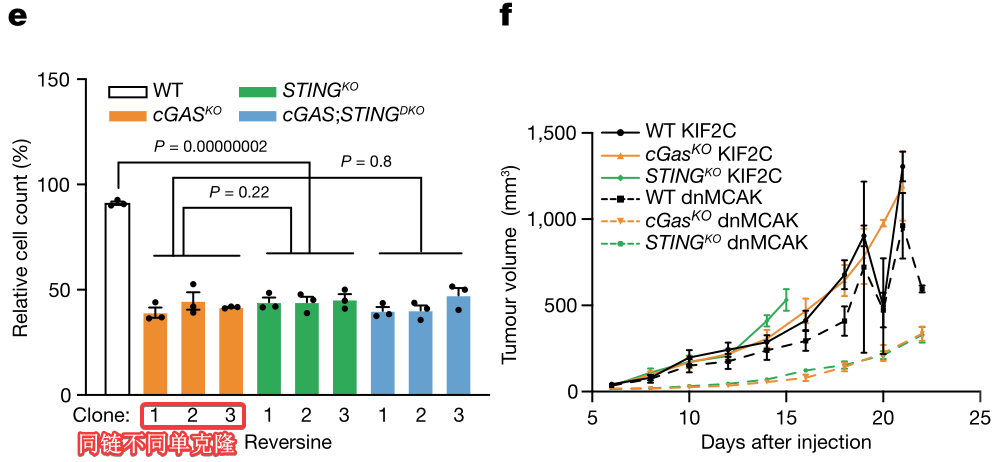
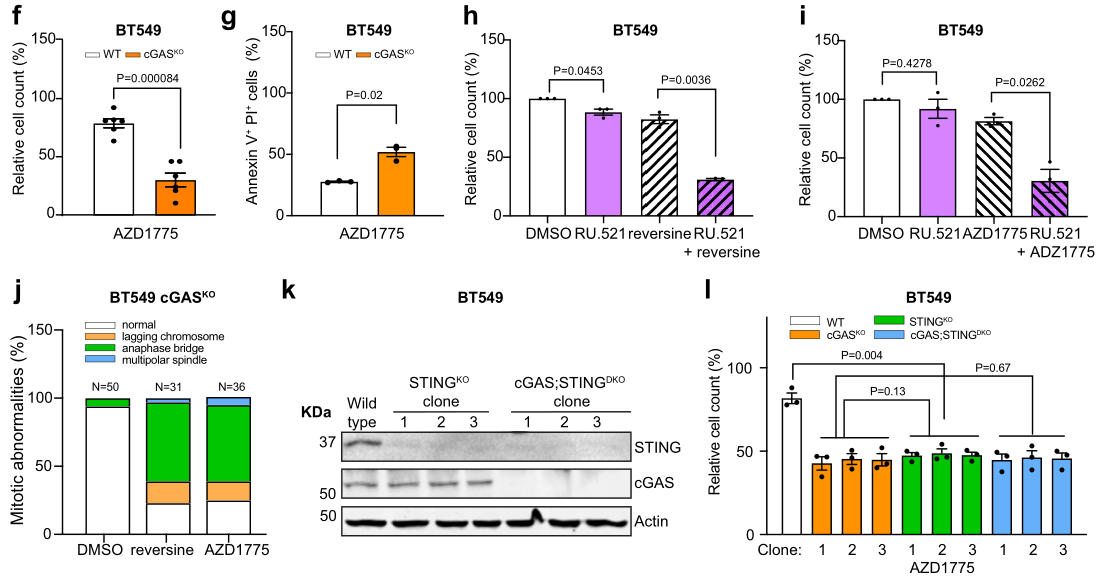
探索机制
为了进一步探索CIN-cGAS-STING轴的下游,研究者首先观察了cGAS-STING的经典下游,主要是转录因子IRF3/STAT1/STAT3等的活性变化。首先,Western Blot检测表明诱导CIN后BT549细胞的cGAS-STING下游信号显著增强:
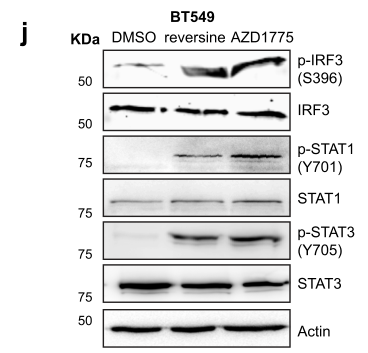
利用cGAS KO/STING KO的细胞系,研究者还进一步表明Reversine促进STAT1/STAT3/IRF3磷酸化的过程依赖cGAS-STING信号,缺少cGAS/STING只能引起较弱甚至是无反应:

此外,研究者基于RNS-Seq进一步挖掘Reversine诱导CIN后抑制cGAS信号时下游分子/通路的改变,发现Reversine诱导BT549细胞的CIN后,cGAS KO介导的IFN–STAT1–STAT3信号减弱比TNF–NF-κB信号更加显著:
这个技巧可以学习一下
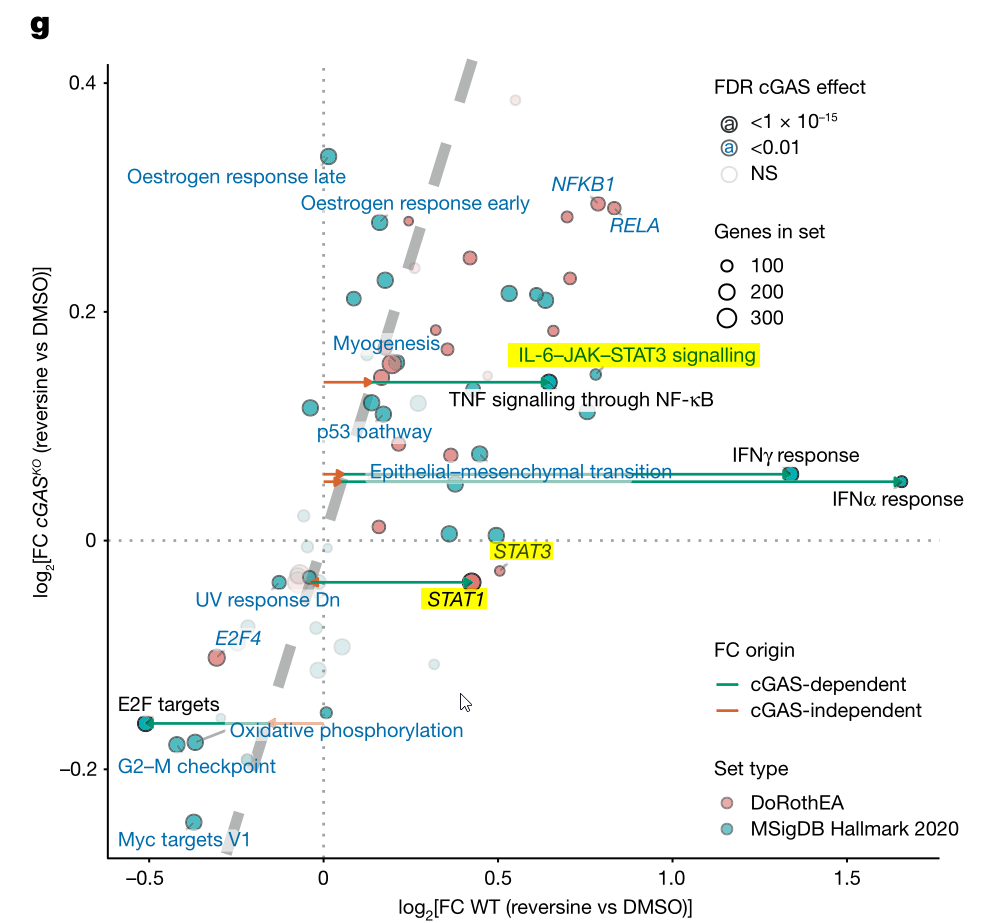
在附图里作者列出更加详细的分析(从基因、hallmarks基因集、TF调节3个方面分析。主要是相对定性地比较。注意作者的实验设计):
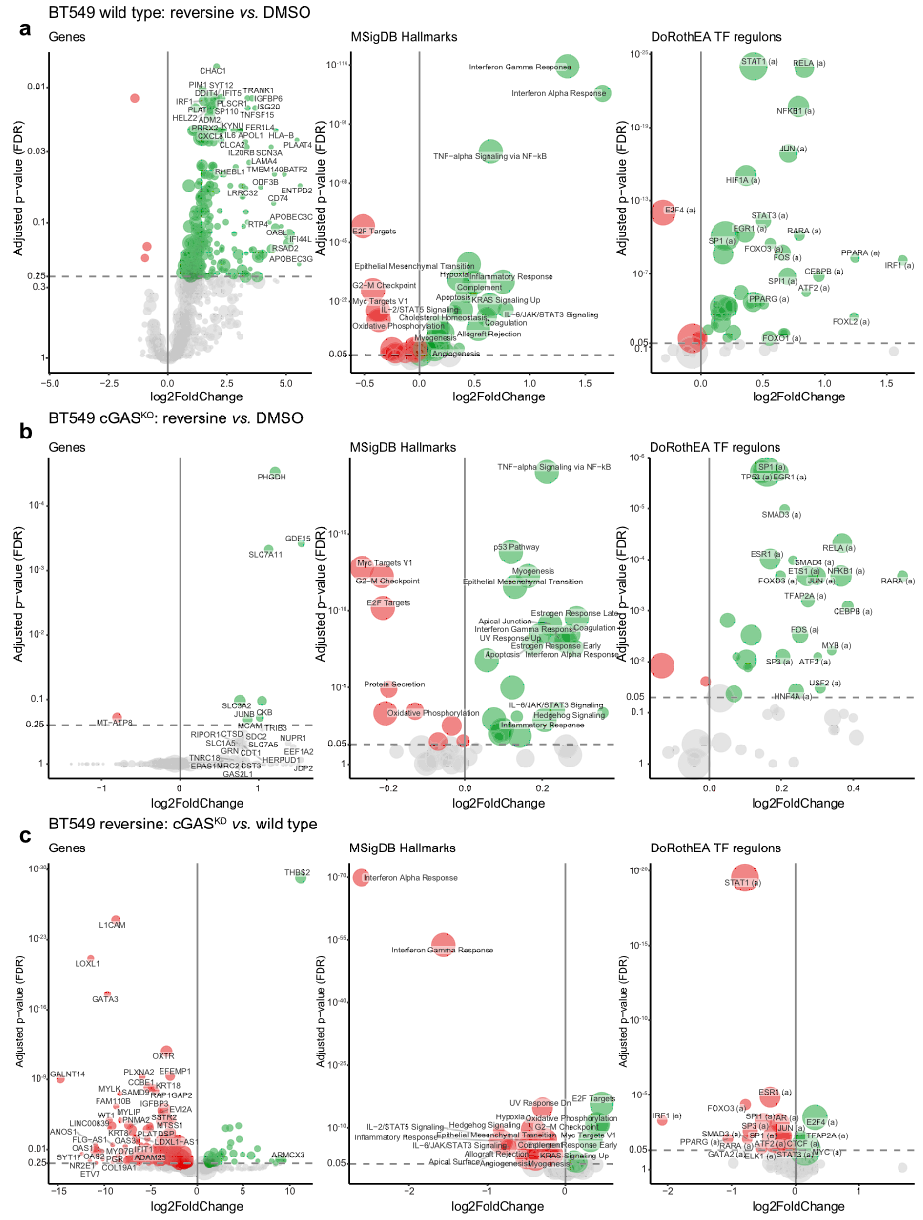
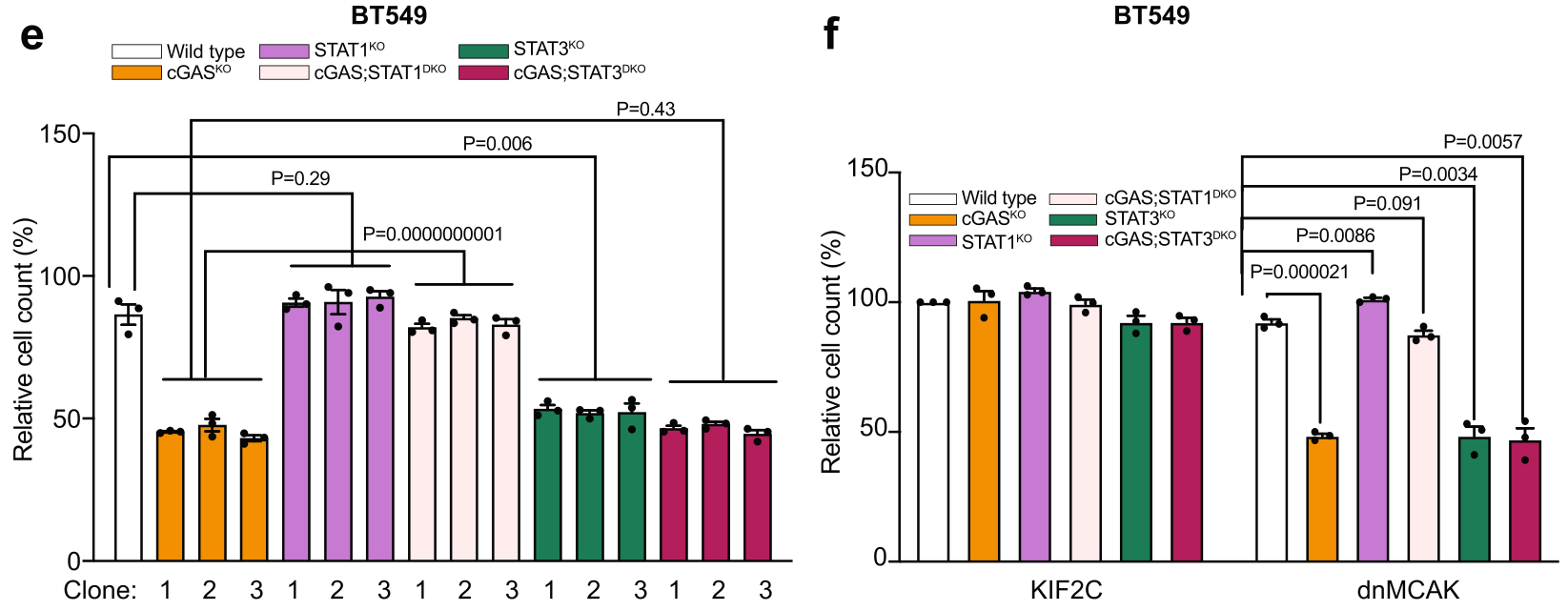
由于CIN肿瘤中cGAS信号缺失会较大地影响IFN–STAT1–STAT3信号,研究者将注意力放在STAT1和STAT3在肿瘤细胞耐受CIN中的具体作用。实现表明STAT1 KO虽不直接影响肿瘤细胞的活性,但STAT1 KO后cGAS KO的CIN增敏效应将不存在;STAT3 KO虽可导致肿瘤细胞对CIN敏感,程度与cGAS KO类似;但两者无明显的协同效应。这表明cGAS-KO所介导的Reversine治疗敏感依赖STAT1激活而不依赖STAT3?
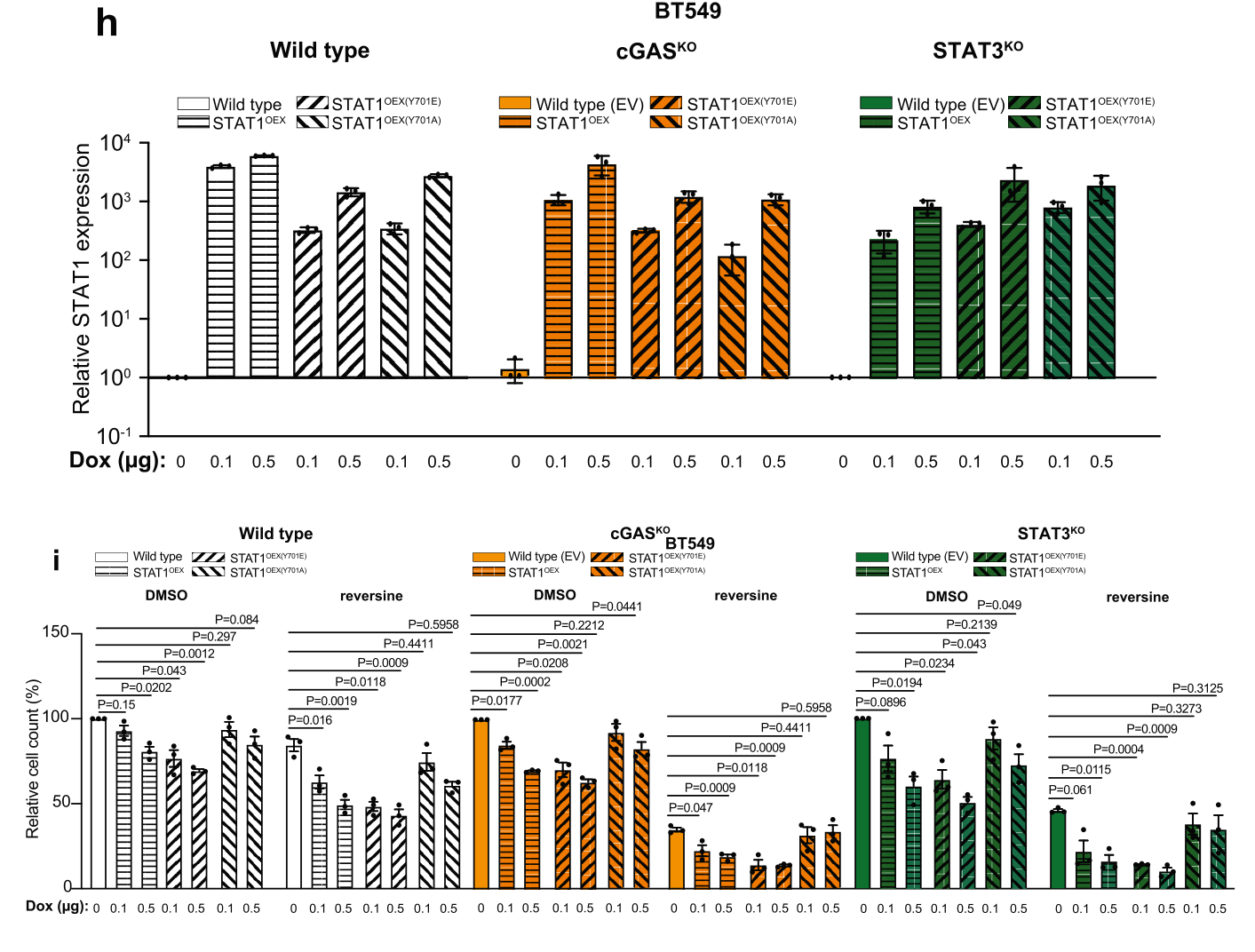
此外,研究者们构建了具有不同活性STAT1突变体的Dox诱导表达模型,发现STAT1Y701E(持续活化型)过表达能在更大程度上增强cGAS KO或STAT3 KO细胞对CIN的敏感性,并表现出剂量依赖性;而STAT1Y701A(不可磷酸化型)则无此效应。这些结果更进一步地证实STAT1激活增强cGAS KO肿瘤细胞对CIN敏感性的重要作用:
扩展论证
NF-kB pathway是机制的另外一条线
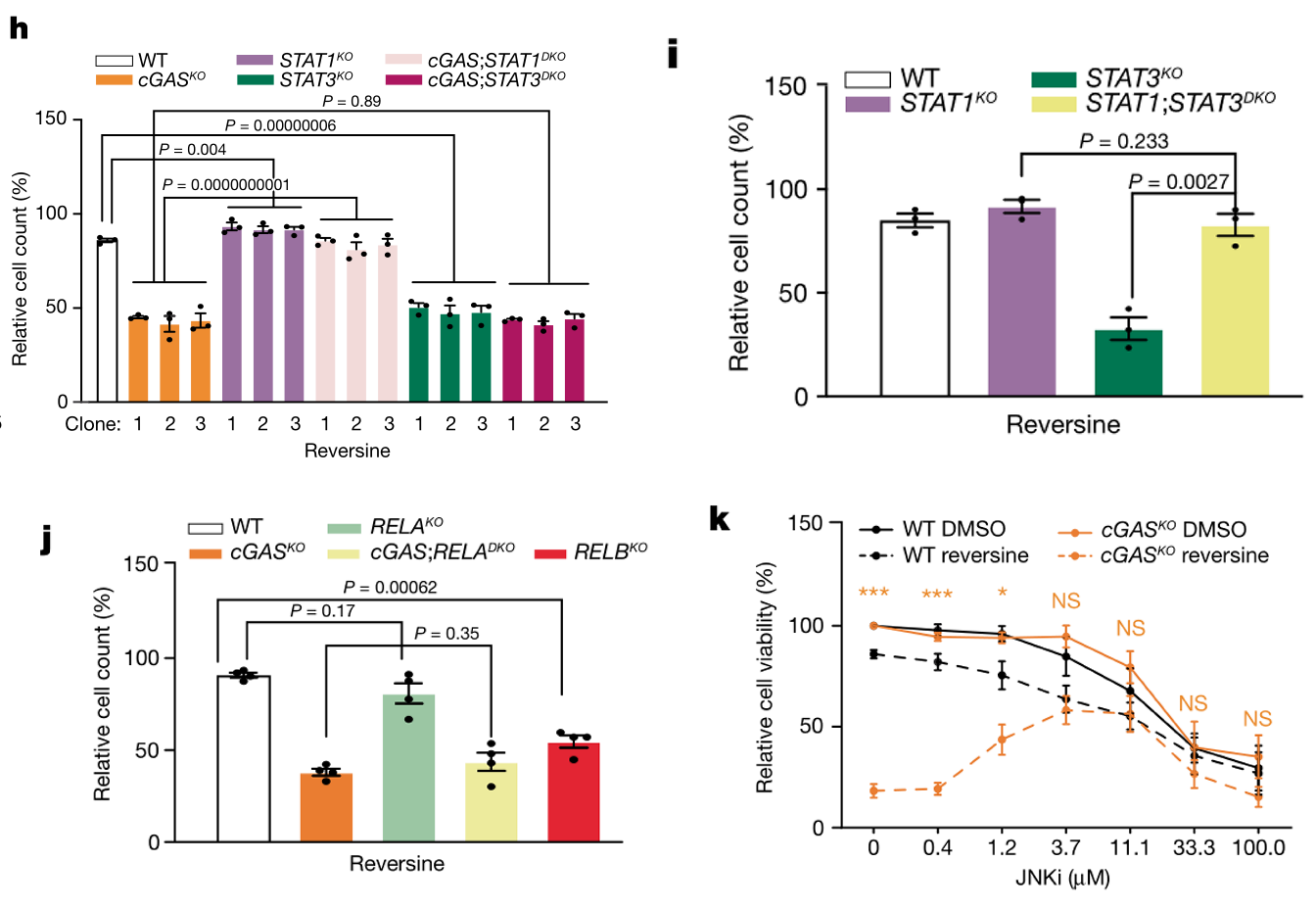
作者还研究了NF-kB的经典/非经典通路,发现NF-kB经典通路信号的缺失(RelA-KO/TRAF2-KO)并不能增强BT549细胞对CIN压力的敏感性,而NF-kB非经典通路信号的缺失(RelB-KO/NIK-KO)则可增强BT549细胞对CIN压力的敏感性。

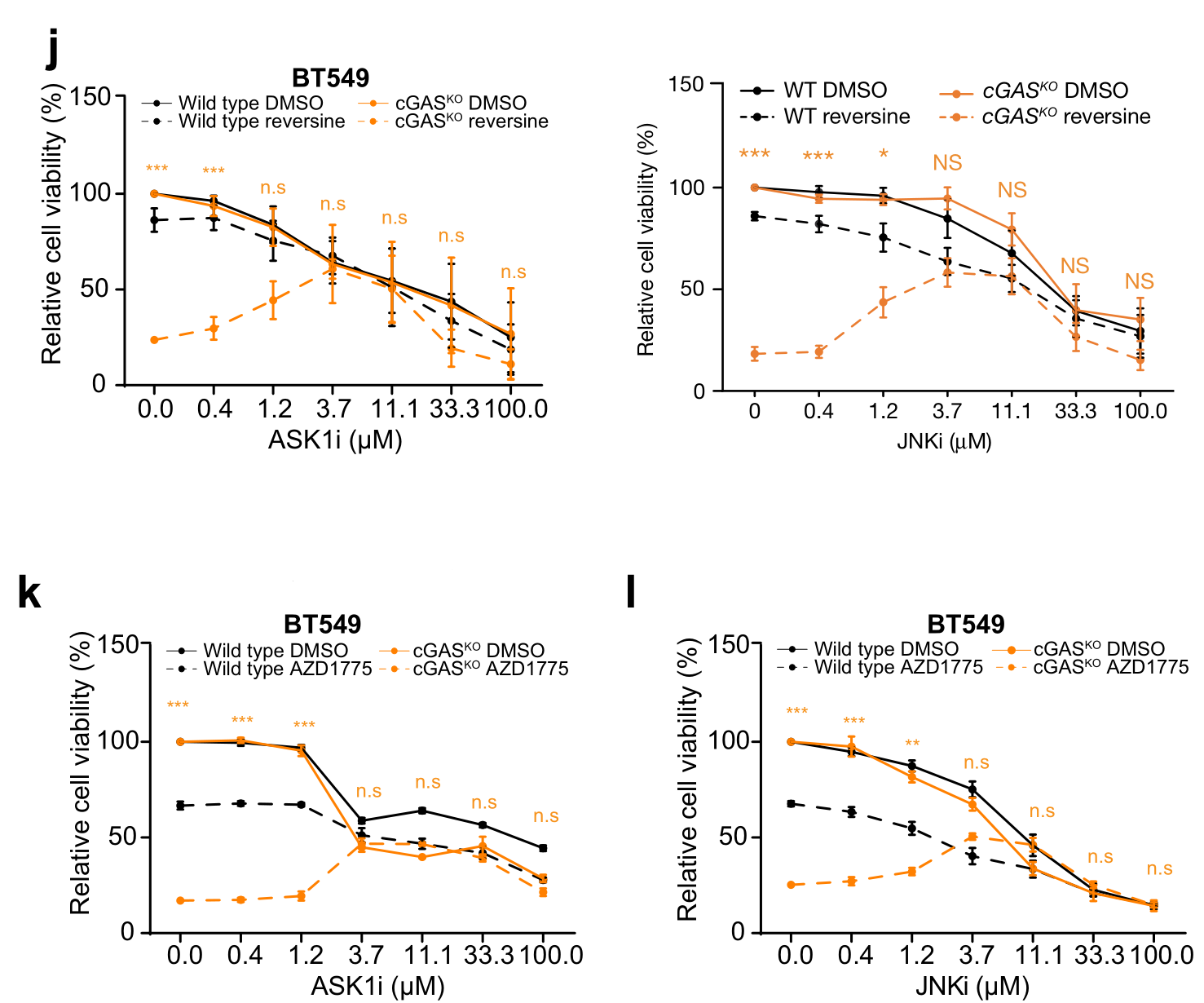
研究者发现低剂量ASK1/JNK抑制剂可增强cGASKOBT549细胞对CIN压力的耐受,这表明CIN诱导cGASKOBT549细胞死亡的过程依赖ASK-JNK信号:
As CIN induces RELB signalling in our model systems (Fig. 1g) and we previously found that CIN-induced TNF–NF-κB signalling can induce apoptosis through ASK–JNK signalling 28 , we next investigated whether inhibition of ASK or JNK would prevent MPS1 and WEE1 inhibitor-induced cell death of cGAS KO BT549 cells. High doses of either the ASK1 and JNK inhibitors NQDI-1 and SP600125, respectively, were toxic to wild-type and cGAS KO cells. By contrast, lower doses of the ASK and JNK inhibitors rescued MPS1 and WEE1 inhibitor-induced cell death in cGAS KO cells (Fig. 1k and Extended Data Fig. 6j–l), which indicates that the cell death observed in CIN-induced cGAS KO cells involves ASK–JNK signalling.
扩展论证2
选同类细胞将流程再走一遍。
除了BT549外,研究者还利用另外一株TNBC细胞——4T1细胞复现了Reversine/AZD1775诱导的CIN压力下的细胞生存依赖于cGAS-STING信号:
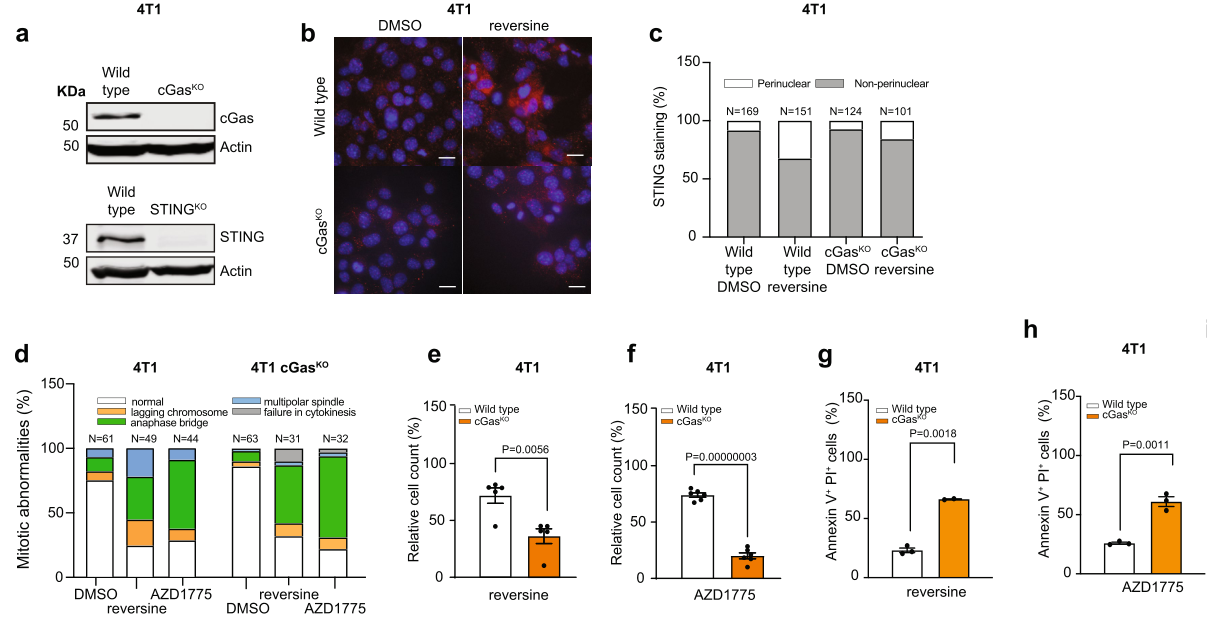
同时,体内外实验和通路分析也表明,cGAS信号缺失可引起相应下游改变并使4T1细胞对急/慢性CIN敏感:
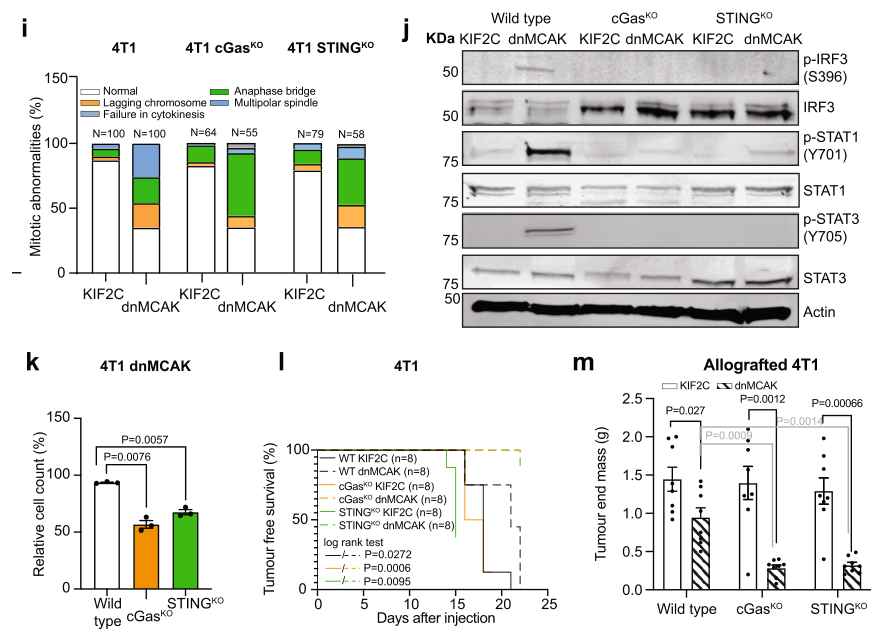
cGAS-STING信号缺失还可引起CCL5、CXCL10(既往研究表明它们是cGAS-STING调节细胞因子)的表达下调:
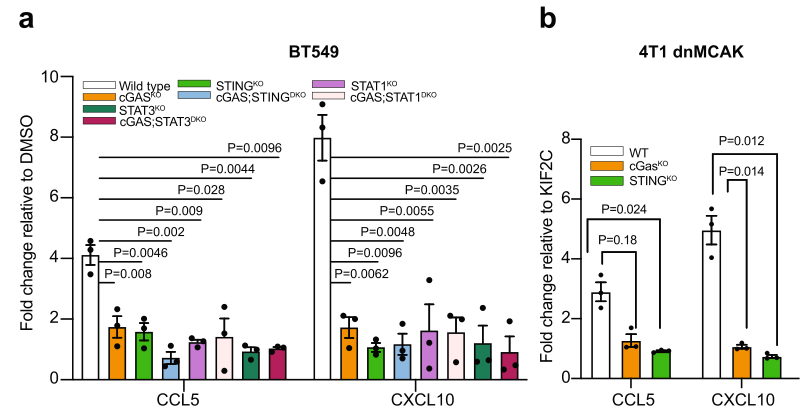
cGAS-STING诱导的IL-6–IL-6R–STAT3信号是CIN型TNBC生存所必需的
STAT1激活在临床上可能不具备操作性,所以作者就研究STAT3通路那边,所以就想到要搞搞IL-6-IL-6R通路?而且IL-6R有FDA-approved drugs,临床转化潜能更强
明确靶点2
通过差异性基因分析,作者发现Reversine处理后细胞IL6表达水平上调(Reversine vs. WT):
这个geom说实话不太合理,实心点属于Cytokine还是cGAS-dependent呢?
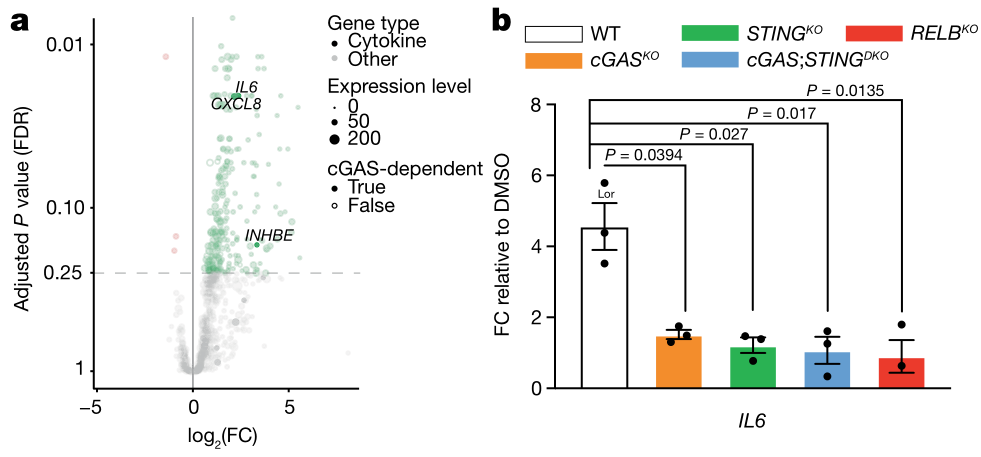
cGAS/STING/RELB基因的KO或DKO后,BT549的活性并不依赖于IL-6;但在Reversine诱导CIN所致BT549细胞活性下降时,使用>0.8ng/ml IL-6即可回复BT579的活性,这表明cGAS/STING信号缺失后,CIN诱导BT549细胞活性下降的过程依赖于IL-6:

扩展论证3
作者还检测了另外一个STAT3信号相关的细胞因子IFNα,结果类似于IL-6,低浓度重组IFNA2可增强cGAS KO细胞在CIN压力下的生存能力。高浓度IFNA2可能通过高度激活STAT1从而促进细胞死亡。

基于多个TNBC细胞系(BT549, MDA-MB-231, MDA-MB-436, E0771)和IL-6信号抑制剂Tocilizumab的体外实验表明IL-6 blockade可增强cGAS信号缺失肿瘤细胞对CIN的敏感性,而非CIN肿瘤细胞则无此效应:
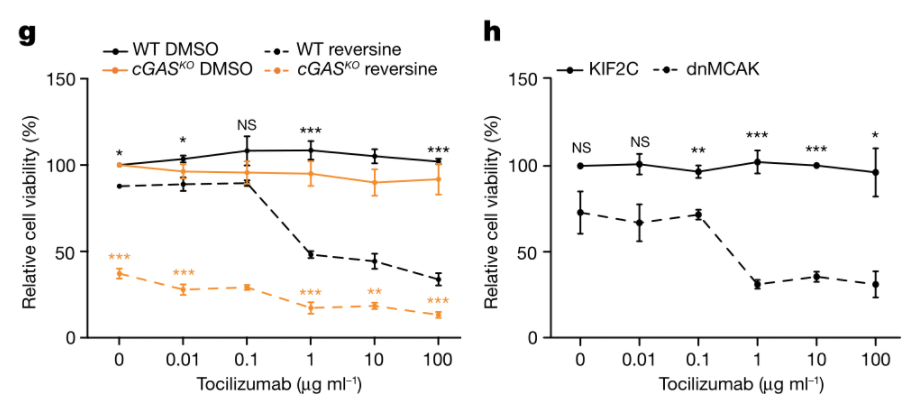

扩展论证4
主要在
诱导CIN这个点玩花样,通过操纵MCAK基因构建慢性CIN-high/low细胞模型
对于CIN-high(dnMCAK OE)、CIN-low(KIF2C OE)的4T1肿瘤细胞的研究也表明IL-6 blockade可增强cGAS信号缺失肿瘤细胞对CIN的敏感性:

类似的,CIN-high肿瘤的核周STING水平、pSTAT1Y701水平均高于CIN-low肿瘤:
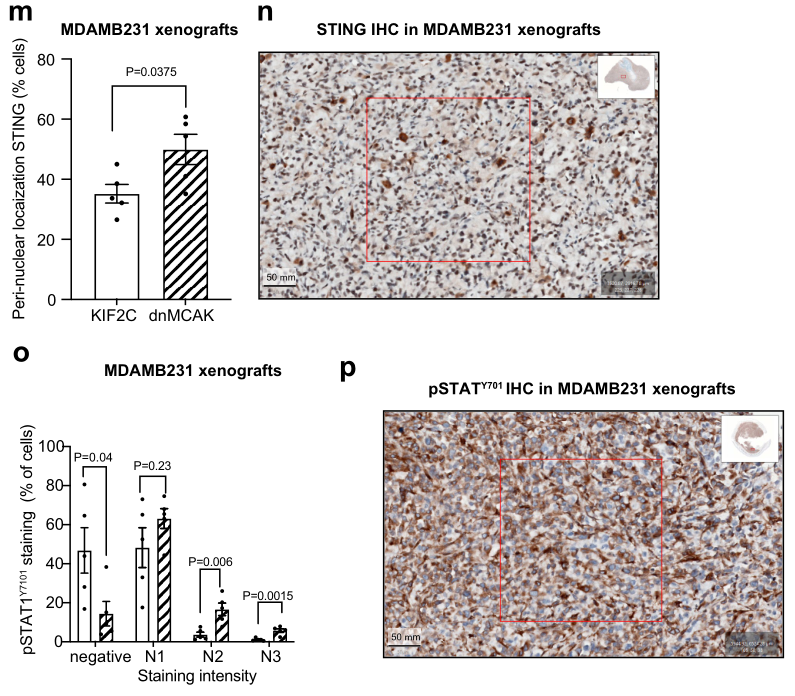
抑制IL-6R可损害CIN型TNBC的生长
体内实验验证一波
靶向治疗
研究者通过体内实验证明CIN-high肿瘤对于IL-6R blockade治疗十分敏感:
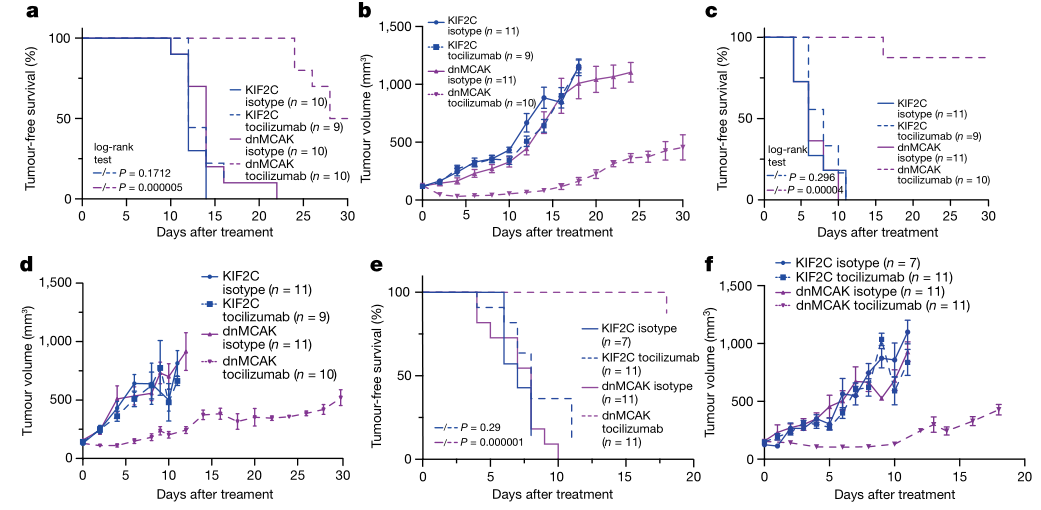
扩展论证5
进一步对TCGA-BRCA数据分析表明在很多ER/PR/Her2阴性、低IFN-γ信号(所谓的Immune-cold)的肿瘤样本中,有相当部分的IL-6信号较强。这个结果暗示IL-6 blockade治疗在ER/PR受体阴性、低IFN-γ信号肿瘤中或有一定的应用前景。
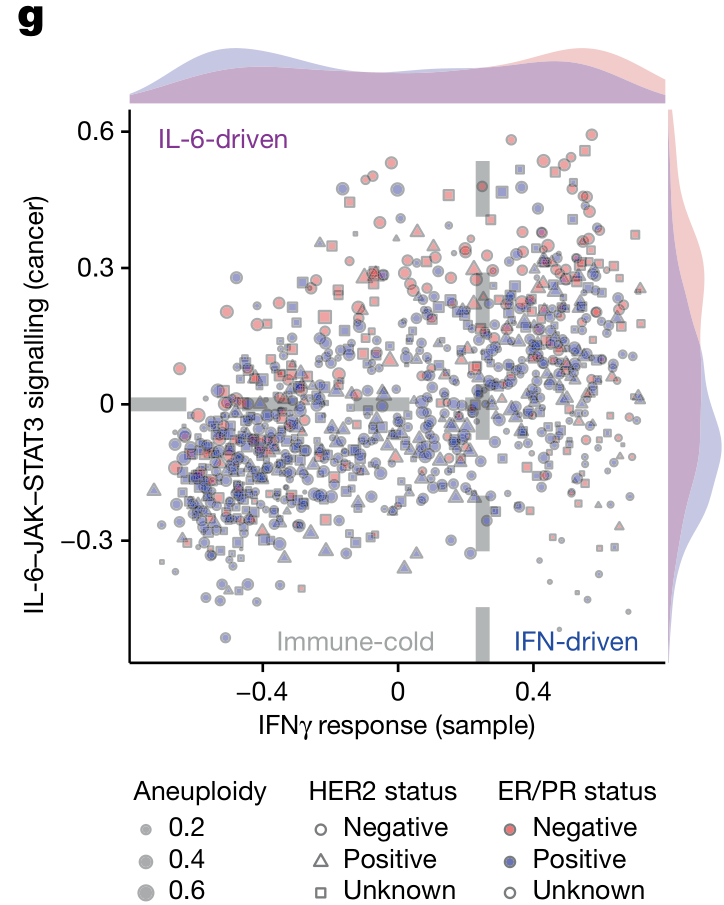
针对TCGA-BRCA亚组的生存分析结果表明:在高倍性/高CIN状态的患者中,肿瘤组织IL-6信号较强的患者预后甚至比immune-cold更差。
是不是可以在泛癌队列里分析一波,看看有什么分子可以和IFN signaling/Aneuploidy相互独立地影响预后?

抗IL-6治疗的泛癌普适性
在泛癌水平上推广结论。
扩展论证6
为了进一步评估CIN与IL-6在其它肿瘤的普适性,研究者观察了CCLE的数据,根据预测初步锁定数个在CIN状态时对抗IL-6信号治疗敏感/耐受的细胞株:
这个预测的标准是什么?
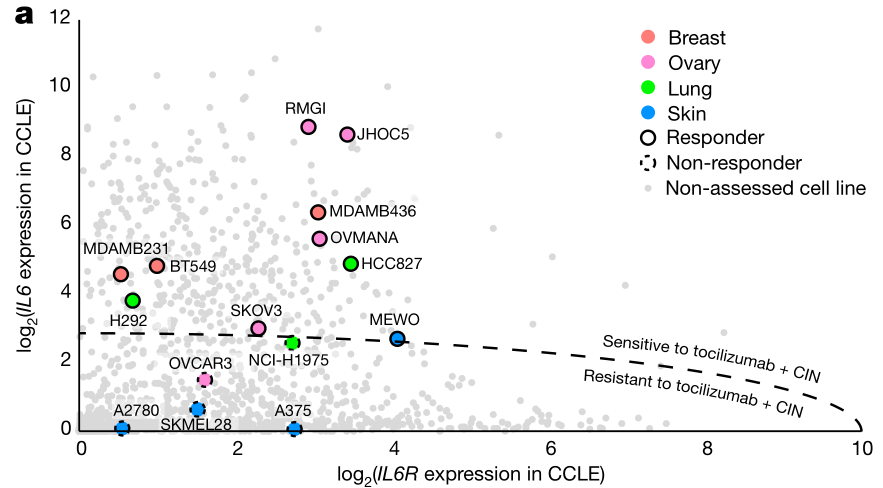
qPCR进一步验证:

进一步的Tocilizumab药敏实验也进一步佐证了预测的结果。比如,NCI-H1975、OVCAR3、A375、SKMEL28在CIN状态下确实对IL-6R blockade不太敏感:

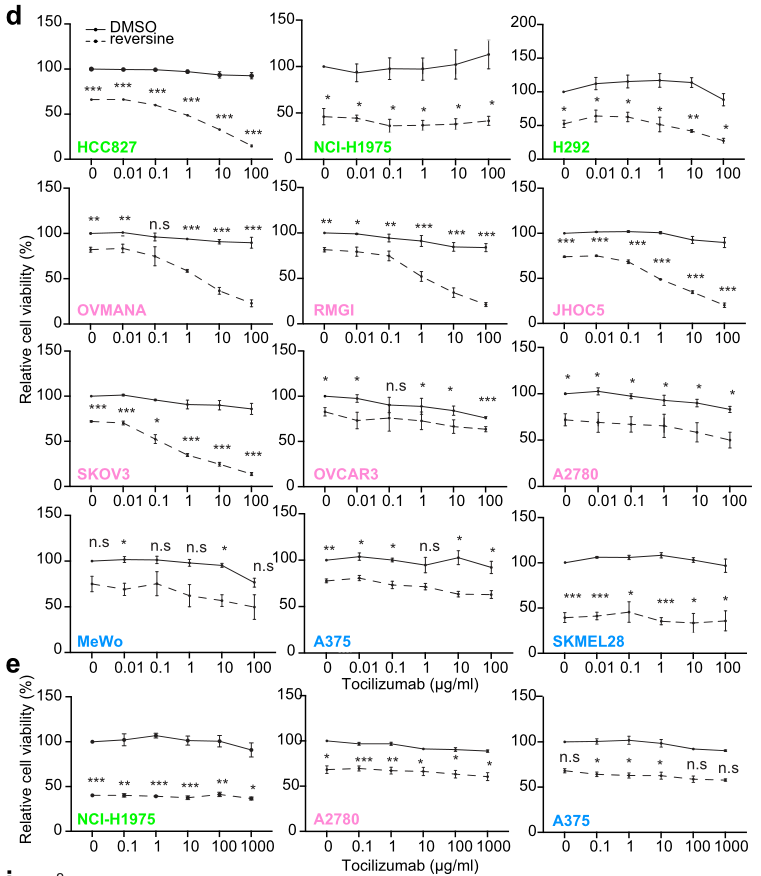
作者利用HCC827细胞进一步在体内研究CIN与IL-6R blockade的关系:
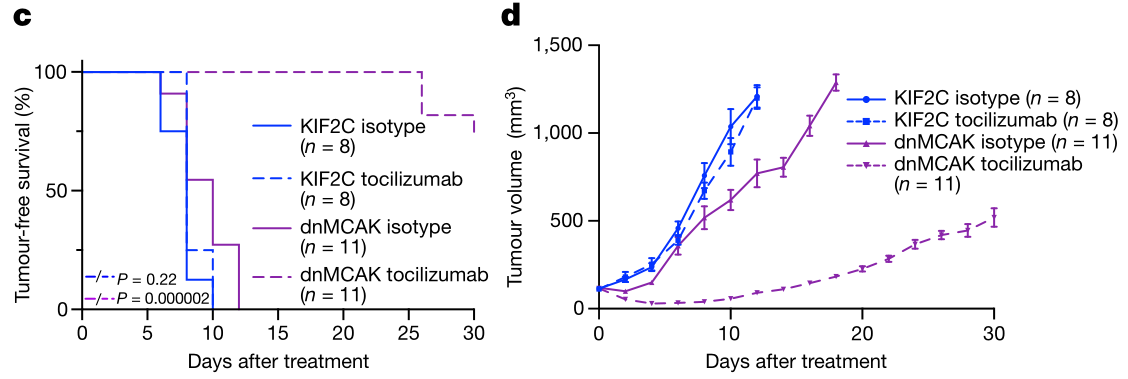
自发T-ALL
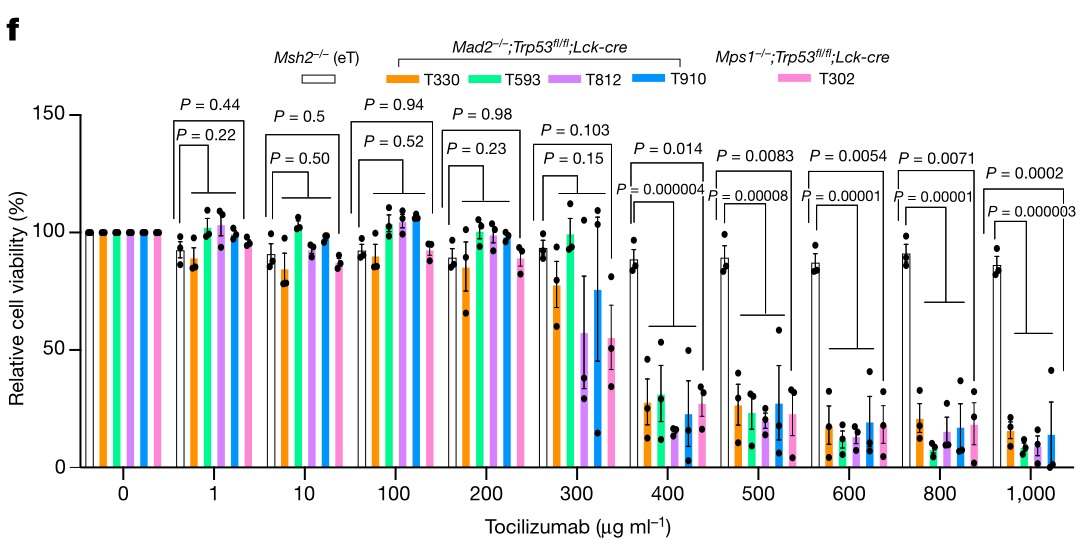
通过Mad2 fl/fl/Mps1 fl/fl ;Trp53 fl/fl ; Lck-cre鼠构建CIN型急性T细胞白血病动物模型,通过单细胞测序的Chromosome copy number分析表明,模型鼠显示出与慢性CIN一致的高度非整倍体和核型异质性,与之对应的Msh2 –/– T-ALL cells则无CIN(eT):

体外实验表明在与原始的、非CIN性T-ALL小鼠肿瘤细胞相比,CIN性T-ALL小鼠的肿瘤细胞对Tocilizumab治疗敏感:
小结
创新性
本文主要论证了靶向cGAS-STING信号在CIN肿瘤中的有效性及具体机制,并挖掘出IL-6/IL-6R信号可作为靶向STAT1/STAT3下游信号的共同靶点,加速了临床上通过阻断IL-6信号治疗CIN肿瘤治疗的进程。
本研究反映了过去20年生物医学技术快速发展的阶段性成果之一。至少在10年前(甚至可能更早),基于二代测序和bulk组织大数据为核心的高通量泛癌研究已经发现CIN型肿瘤并归纳了其基本特征。所以CIN型肿瘤并不是一个新的发现。比如在胃癌中,除了CIN型,常见的分子分型还包括MSI型、EBV型和GS型。不过,当时人们还不清楚这些分型如何指导肿瘤患者的临床治疗——因为它们通常是关于肿瘤基因组的宏观描述,并不是某个简单的单基因突变。后来,随着免疫检查点抑制剂(ICIs)在肿瘤治疗领域大放异彩,人们发现EBV型和MSI型肿瘤对于ICIs治疗特别敏感,这可能与较高的肿瘤突变负荷(TMBs)导致的肿瘤的高免疫原性有关(当然具体的机制也仍在研究当中)。针对MSI或CIN肿瘤的特异性疗法让肿瘤分子分型焕发出新的生命力,与它们相关的系列研究正在逐渐地影响着临床治疗决策。
与传统的分子生物学研究不同,分子分型其实比较依赖于现代计算机技术、高能量测序技术、生物大数据(特别是real-word data)及其算法等新型技术的突破。继2015年前后,近期(2022年)Nature再次推出一些CIN、CNV的泛癌研究,估计是大佬们在肿瘤组学研究中又有一波新的大发现,拿到全文后有机会再向童鞋们介绍。另外,我也完全相信诸如Single Cell Sequencing之类的新技术会在未来更加深刻地改变生物医学的研究。
值得一提的是,cGAS-STING信号通路的发现也蛮久远了;而且首先发现也不是在肿瘤领域,而是研究微生物性疾病和细胞天然免疫研究领域。在过去20年里,cGAS-STING信号的机制研究得也比较透彻,cGAS-STING-I型IFN/NF-κB轴的机制算是比较经典。从这个角度上看,本研究创新的点其实并不多。我估计将IL-6R blockade治疗肿瘤的研究应该很多,但指明在CIN型肿瘤对IL-6R blockade治疗敏感的研究应该不多,所以它确实是一项有望改写临床指南的研究。再加上夯实的实验验证,其发表在CNS上也不太令人惊讶。
实验设计
我估计作者很早就确定了这个文章的框架,至少有一些IL-6R blockade治疗CIN肿瘤的体外实验结果就已经确定了。在机制研究上,本文确实没有很多新的点;但这篇论文的临床转化能力确实太强,毕竟IL-6R抑制剂——Toclizumab可是一款正儿八经的FDA-approved药物!只不过之前的适应症是类风湿关节炎、全身性幼年特发性关节炎(SJIA)、多关节幼年特发性关节炎(PJIA)、巨细胞动脉炎、细胞因子释放综合征、系统性硬化症相关间质性肺病之类的自身免疫性疾病,还没有肿瘤适应症。此文一出,抗IL-6治疗的适应症又有可能要扩展了,如果临床实验的结果好的话,说不定这事就成了!Genentech公司的主管看到这个研究估计睡觉都要笑醒了。总之,我觉得本文特点可以这样总结:不好意思,临床转化真系大晒!

尽管如此,CNS级别论文实验论证的深度和广度一般都有保障的,也不是一般的文章能比,本文也不例外。比如:
- 诱导CNI肿瘤:作者除了使用Reversine/AZD1775构建急性CIN模型,也通过构建KIF2C/dnMCAK-OE细胞来构建CIN模型。不知道研究CIN肿瘤的人里是不是常规操作。
- 多种细胞:除了多个TNBC,后面还测试了很多其它癌种的细胞。
- 变量控制:多数目标基因使用了knockout甚至是double knockout,在研究STAT1时还使用了Dox诱导的剂量依赖性过表达。
- 机制广度和深度:基于cGAS-STING,机制研究走了STAT1/STAT3两条线,这也是蛮难驾驭的。
- 生物大数据:有部分数据,但个人觉得并不太关键,只是锦上添花的作用。
- 动物模型:移植瘤模型、条件性敲除鼠,CNS常规操作吧,不吹不黑。
总之,这个文章还是有很多值得学习的地方,以后有什么心得再回来补充!
---------------
完结,撒花!如果您点一下广告,可以养活苯苯😍😍😍
